MSCs可历史上调颗粒细胞中AMH激素和促卵泡激素受体的表达,抑制颗粒细胞凋亡和卵泡闭锁,慷慨卵巢成果的规复;临床级MSCs的生产需要大批的细胞,但体外高代MSCs扩增大约造成细胞转化,凭证疾病的重要程度,必需确定很好剂量和特定给药时间。
目前来自骨髓、脂肪组织、脐带、脐带血、胎盘、羊水、子宫内膜、脐带沃顿胶和经血等多种来源的MSCs在试验中获得了成功。

以下为原文:
间充质干细胞在卵巢成果规复中的用途
随着再生医学的发展,间充质干细胞(mesenchymal stem cells,MSCs)作为一种规复卵巢成果的方法受到人们的正视。据报道,来源于骨髓、脂肪、脐带血、经血和羊水的MSCs可改进卵巢成果。鉴于先前的研讨和这方面的进展,人们对利用MSCs规复卵巢成果的期望越来越高。本文综述了近年来MSCs在不孕或原发性卵巢成果不全患者中的埋伏应用研讨,包含抗肿瘤治疗惹起的情况。
间充质干细胞的特性
间充质干细胞(Mesenchymal stem cells,MSCs)是一类来源于人和哺乳动物骨髓和骨膜的细胞,在培养过程中能够被划分辨别和扩增,同时结合体外诱导造成多种中胚层表型和组织的能力。缩写MSC能够清楚为间充质基质细胞,多醒目细胞,间充质祖细胞,骨髓基质细胞、骨髓间充质干细胞、间充质前体细胞、骨骼干细胞和多能间充质干细胞.
为了前进术语的清楚度,国外细胞治疗学会(ISCT)将间充质干细胞定义为多能间充质基质细胞,建议这应指来自具有可塑性粘附特性的基质组织的细胞,保存术语“间充质干细胞”来表示现实上具有干细胞两个基本特性(自我更新和向下分化多个谱系的能力)的亚群[5]。
ISCT提出了定义MSCs的三个尺度。首先,MSCs必需在尺度培养条件下具有可塑性。其次,95%以上的MSCs必需表达CD 105、CD73和CD90,而缺乏CD45、CD34、CD14或CD11b、CD79a或CD19和人类白细胞抗原(HLA)Ⅱ类的表达。第三,这些细胞必需能够在尺度的体外分化条件下分化成成成骨细胞、脂肪细胞和软骨母细胞[5]。
间充质干细胞来源于成人或婴儿体内的多种组织,包含脂肪组织、外周血、脐带血、脐带血、脐带、脐带膜、脐带静脉、华顿脐带果冻、胎盘、基底膜蜕膜、粗面韧带、羊水液等,羊膜、牙髓、人胎盘绒毛、胎膜、经血、母乳和尿液[6]。
MSCs具有壮大的调理免疫反应的能力,包含抑制T细胞增殖,影响树突状细胞成熟和成果,抑制B细胞增殖和终末分化,以及调理别的免疫细胞,如自然杀伤细胞和巨噬细胞[7]。MSCs在细胞治疗中的另一个用途是归巢和跨内皮细胞迁徙。在循环中,MSCs历史血管系统,历史趋化因子(C–CC motif)、粘附分子(P-选择素和VCAM-1)和基质金属卵白酶(MMPs;MMP-2和膜型1 MMP)转运到损伤部位[8]。MSCs修复受损的组织部位后,它们与片面刺激亲切关联,如恶臭细胞因子、Toll样受体的配体和低氧,这能够刺激MSCs产生大批的发展因子,用于组织再生的多种成果[8 ]。基于MSCs的这些用途,Caplan建议将MSC的缩写重新清楚为“医学信号细胞”
卵巢成果与卵巢早衰
卵泡是卵巢的成果单位,由卵母细胞及其支持细胞组成,如颗粒细胞、卵泡膜细胞和基质细胞。卵泡中的细胞每月释放一个卵母细胞,从而产生生养能力,并产生雌二醇和孕酮等激素,以结合妇女的整体健康和结合妊娠[10]。
卵巢早衰(POF,又称原发性卵巢成果不全)是一种隐秘而复杂的疾病。POF的患病率为35岁以下妇女的250分之一,40岁以下妇女的100分之一。POF最重要的机制是滤泡成果窒碍和滤泡耗竭[11]。
诚然POF的病因尚未完全阐明,但遗传、内渗透、旁渗透、线粒体成果窒碍和代谢成分可影响卵泡池和卵母细胞的质量[12]。
近年来,化疗造成的POF已成为抗癌治疗的要紧长期不良反应,这种治疗增加了不孕和退行性健康问题的风险。这种对化疗的反应无妨年轻女性的一个分外问题,因为卵巢储备的丧失与女性不育的风险亲切关联。抗癌药物发扬卵巢毒性的确切机制尚未完全建立(13),它似乎取决于药物的对照和所测试的细胞对照[14 ]。基质细胞和颗粒细胞尤其受到大多数抗癌药物历史凋亡的激烈影响。已知卵母细胞历史困绕它们的基质和颗粒细胞受到间接毒性的影响。
环磷酰胺(CTX)是一种烷基化剂,可诱导活跃增殖细胞(如颗粒细胞和基质细胞)DNA的双链断裂,卵母细胞也会受到CTX和别的抗癌药物的损伤[13]。
然而,另一个有趣的注释是,原始卵泡没有增殖,因此对DNA损伤不太敏感。处于静息状况或激活状况的原始卵泡被发现受细胞内磷脂酰肌醇3激酶(PI3K)-Akt-mTOR信号通路掌握[15]。磷酸酶和张力素同源物(PTEN)是PI3K的可逆抑制剂,已知是人类的肿瘤抑制因子[16]。
抗癌药物治疗如CTX或顺铂被发现历史过度渗透造成原始卵泡衰竭[17],卵母细胞特异性PTEN缺失造成小鼠模子中原始卵泡池过早激活[18]。
因此,对于回收化疗的育龄妇女来说,结合生养能力和卵巢成果应被视为一个重要问题。保存生养的几种选择,如胚胎冷冻保存、成熟卵母细胞或卵巢组织。然而,大多数方案都是在抗癌治疗前保存生养能力。因此,有必要探讨规复卵巢成果的大约途径。
MSC治疗与卵巢成果规复
MSC治疗被以为是治疗女性不孕症或规复卵巢成果的新选择。
许多研讨证实了在POF动物模子中,从不同细胞来源获得的MSCs对卵巢成果的保护用途(表1)[19-48]。这些
与别的形式的细胞治疗同样,有两种不同的给药方法被考虑用于间充质干细胞规复卵巢成果。小鼠和大鼠模子中引入了尾静脉注射,卵巢片面注射技术也获得了广泛发展[50]。在用抗癌药物化疗惹起的卵巢成果衰竭中,发现MSCs移植可诱导卵巢成果规复,包含雌二醇的产生和卵巢结构的改进[30,33]。
MSCs对CTX或顺铂等抗癌药物诱导的基质细胞或颗粒细胞凋亡具有保护用途(表1)。MSCs产生的某些细胞因子,包含VEGF、HGF和IGF-1,大约在体内抑制颗粒细胞凋亡和上调B细胞淋巴瘤-2[51]。
间充质干细胞的另一个预期机制是其抗纤维化用途。卵巢纤维化与某些细胞因子相关,包含基质金属卵白酶、基质金属卵白酶组织抑制剂、转化发展因子-1、血管内皮发展因子和内皮素-1。MSCs可抑制fb细胞增殖,减少细胞外基质的沉积[51]。
血管生产是卵巢规复的重要机制。血管内皮发展因-2,分外是来自MSCs的血管生产素诱导复活血管造成,慷慨受损卵巢组织的血液灌入[44,51]。人胎盘来源的MSC移植后历史调理调理T细胞和关联细胞因子规复POF小鼠卵巢成果[29]。将人羊膜间充质干细胞移植到自然苍老小鼠体内12~14个月后,移植的间充质干细胞历史渗透表皮发展因子和HGF在抑制卵巢苍老中发扬了重要用途[22]。然而,MSC移植慷慨卵巢成果的机制有待进一步研讨。
表1:MSC支持的卵巢成果研讨
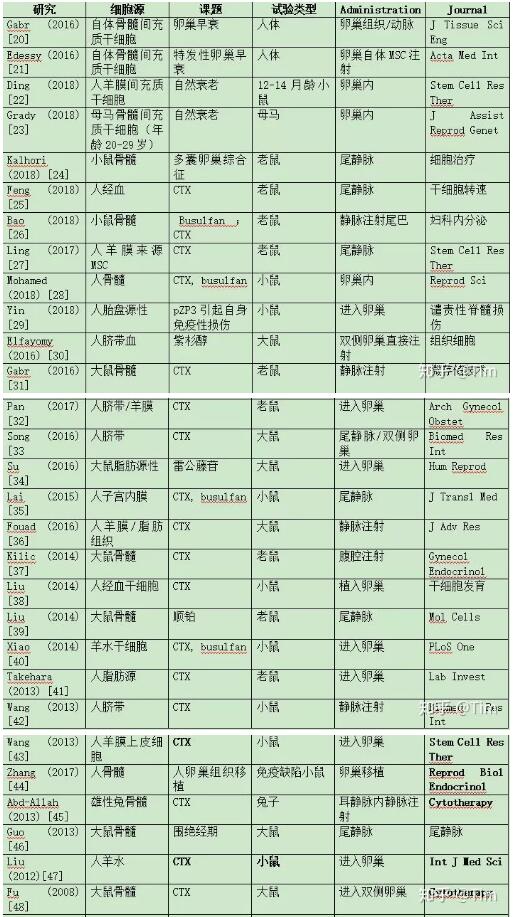
MSC, 间充质干细胞;CTX, 环磷酰胺.
规复卵巢成果的新候选MSCs
临床应用需要多剂量的间充质干细胞,剂量范围为每公斤体重1-5百万个细胞[52],在动物试验中,每只老鼠或大鼠的细胞数量为1百万至5亿个单位。然而,从成人组织获得MSCs需要适宜的供体,在大多数情况下,必需进行侵入性手术。别的,长期培养大约增加诱发染色体畸变和异质细胞群的风险,使其难以尺度化协议[52]。
人胚胎干细胞(hESCs)来源于囊胚的内部细胞团,具有多潜能,可分化为三个胚层。少许研讨表明,MSCs能够从hESCs中获得,它们表达MSC表面标志物,并分化为三个胚层(如软骨细胞、成骨细胞和脂肪细胞)[53]。别的,据报道,这些细胞在体外试验中发扬免疫调理用途[54]。hESC来源的MSCs相当于骨髓或脂肪来源的MSCs,使其成为规复卵巢成果的MSCs的替代来源[52]。然而,涉及人类胚胎应用的伦理问题仍然存在,对于移植过程中hESCs不受欢迎、意外或不受掌握的迥异的关注仍在讨论中。然而,基于hESCs和hESC衍生MSCs治疗种种疾病的临床试验曾经启动[55]。诱导多醒目细胞(IPSC),无妨MSCs的另一个来源。iPSCs能够历史微创手术获得,幸免了胚胎应用和hESCs的伦理问题。别的,应用自体或HLA匹配的iPSC系大约使免疫问题最小化[56,57]。
MSCs的另一个候选者是外体,外体是由细胞渗透的膜质生物纳米粒。它们在系统中循环,佩戴mRNA、长的非编码RNA、microRNA、卵白质和脂质。在肿瘤生理学中,细胞增殖、凋亡、细胞因子产生、免疫调理和转移等过程中发现了对胞外体的刺激或抑制成果结果[58]。MSC介导的细胞治疗中的外体在许多疾病模子中被发现,并被发现慷慨成果规复[59]。人脂肪或脐带血MSCs来源的外体改进了卵巢早衰小鼠模子的卵巢成果[60,61]。然而,在外显子划分辨别、表征和去管理技术方面的少许尺度化问题仍然需要解决[59,62]。
MSCs的安全问题
间充质干细胞的安全性问题应该获得解决,因为在给药后,观察到轻细的不良反应。最重要的不良反应是长期培养的MSCs慷慨了肿瘤的发展和转移。临床级MSCs的生产需要大批的细胞,需要体外扩增,但高代MSCs大约造成细胞转化。凭证疾病的重要程度,必需确定很好剂量和特定给药光阴。有必要深入了解间充质干细胞的调控机制,并制定相应的管理方法。
结论
MSCs已成为细胞治疗临床应用中最有效的细胞对照。多发性退行性疾病和少许免疫关联疾病被报道对MSC移植有反应。来自骨髓、脂肪组织、脐带、脐带血、胎盘、羊水、子宫内膜、脐带沃顿胶和经血等多种来源的MSCs是成功的试验工具。
据文献报道,MSCs可历史上调颗粒细胞中AMH激素和促卵泡激素受体的表达,抑制颗粒细胞凋亡和卵泡闭锁,慷慨卵巢成果的规复。目前正在进行的骨髓间充质干细胞再生利用以规复卵巢成果的研讨,能够为POF患者和不孕或亚生养期妇女带来希望。


